2020進口保健食品備案全景透視 日本、德國、丹麥首備成功背后的市場機遇與合規邏輯
2020年,中國進口保健食品備案工作繼續穩步推進,市場準入與監管體系日益成熟。其中,日本、德國、丹麥等國家在特定產品類別上實現“首備成功”,成為行業關注的焦點。這不僅標志著相關產品正式獲得進入中國市場的“通行證”,也折射出全球保健食品產業格局的演變與中國消費者需求偏好的變遷。對相關備案信息進行系統梳理與深度分析,對把握行業趨勢、理解監管導向具有重要意義。
一、2020年進口保健食品備案總體態勢
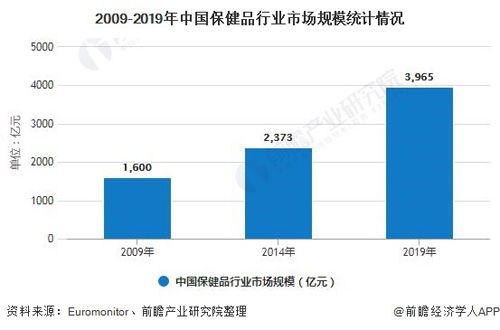
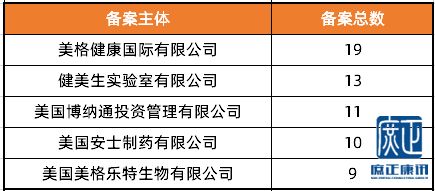
根據國家市場監督管理總局(SAMR)及相關數據庫公開信息,2020年進口保健食品備案數量保持穩定增長。備案產品仍集中于營養素補充劑(如維生素、礦物質)等法規相對清晰、原料目錄明確的類別。備案主體以在華注冊的境外生產商或其境內責任單位為主,顯示出品牌方對中國市場長期投入的決心。監管層面,延續了“備案制”與“注冊制”雙軌并行模式,對使用《保健食品原料目錄》及《允許保健食品聲稱的保健功能目錄》內成分與功能的產品實施備案管理,流程效率較高。
二、日本、德國、丹麥“首備成功”案例解析
1. 日本:精細化營養與原料優勢的體現
2020年,日本某知名品牌以“膠原蛋白肽”為主要成分的飲品成功完成備案。這并非新原料,但日本企業在產品配方精細化、口味劑型創新及品質控制方面表現突出。該備案成功,體現了中國市場對具有美容、關節健康等宣稱的特定功能產品,以及日本在海洋生物提取物、發酵技術等領域原料口碑的認可。日本保健食品素以“精細”、“溫和”、“劑型多樣”著稱,其備案策略往往聚焦于其優勢原料(如肽類、特定植物提取物)與差異化的產品形態。
2. 德國:科學背書與“品質可靠”標簽的強化
德國成功備案的產品中,以復合維生素礦物質片劑、Omega-3脂肪酸類產品為代表。德國保健食品工業與藥學傳統結合緊密,強調科學實證與生產質量管理。其“首備成功”的產品,往往附有嚴謹的科學研究支持,生產工藝符合歐盟及國際高標準。這精準對接了中國中高端消費群體對“德國品質”的信賴,尤其是在母嬰營養、基礎營養補充等領域。德國產品的成功備案,強化了其在華“科學、嚴謹、可靠”的品牌形象,為后續同類產品進入鋪平了道路。
3. 丹麥:益生菌領域的領先地位與市場先機
丹麥在益生菌及相關制品領域的備案取得突破,具有標志性意義。依托全球領先的菌種研發與生產企業,丹麥備案的特定菌株益生菌產品成功進入目錄并完成備案。這得益于中國對益生菌類保健食品的法規路徑逐漸明晰,以及市場對腸道健康、免疫支持等功能需求的激增。丹麥“首備成功”,不僅鞏固了其在全球益生菌供應鏈中的核心地位,也抓住了中國消費者健康意識提升帶來的早期市場紅利。
三、備案信息背后的行業趨勢與挑戰分析
趨勢洞察:
1. 來源地多元化與優勢細分:備案成功的國家不再局限于傳統的美澳大國,日、德、丹等國的成功,顯示出市場正根據各國產業特長進行細分領域的深耕。
2. 功能訴求精準化:備案產品功能集中指向美容(抗衰老)、關節健康、腸道健康、基礎營養補充等,與都市人群的健康痛點高度契合。
3. “科學證據”與“原料溯源”成為關鍵:無論是德國的科研背書,還是丹麥的菌株專利,抑或日本的原料工藝,提供可信的科學依據和透明的原料信息,是贏得監管與消費者雙重信任的核心。
挑戰提示:
1. 法規適應性:各國產品配方習慣與中國的《原料目錄》、《備案細則》需要精準對接,任何成分、用量、聲稱的偏差都可能導致備案失敗。
2. 市場同質化競爭:基礎營養素補充劑等備案類別進入門檻相對較低,市場競爭激烈,“首備”帶來的窗口期紅利可能縮短。
3. 消費者教育成本:新產品、新功能需要大量的市場教育,備案成功僅是第一步,品牌建設與渠道拓展同樣至關重要。
四、結論與展望
2020年日本、德國、丹麥等國在進口保健食品備案上取得的成功,是各國產業優勢與中國市場法規、消費者需求成功對接的縮影。它預示著中國進口保健食品市場正朝著來源地更多元、產品更細分、科技含量更高的方向發展。對于行業參與者而言,深入分析備案數據,洞察監管風向,結合自身優勢選擇精準的品類與功能賽道,并構建從原料到聲稱的完整科學證據鏈,是在這一市場贏得長期發展的必由之路。隨著備案目錄的動態調整與擴充,以及跨境電子商務等新渠道的融合,進口保健食品市場的信息處理與分析將變得更加重要,成為企業戰略決策不可或缺的一環。
如若轉載,請注明出處:http://www.utrxndq.cn/product/31.html
更新時間:2026-04-30 07:48:16